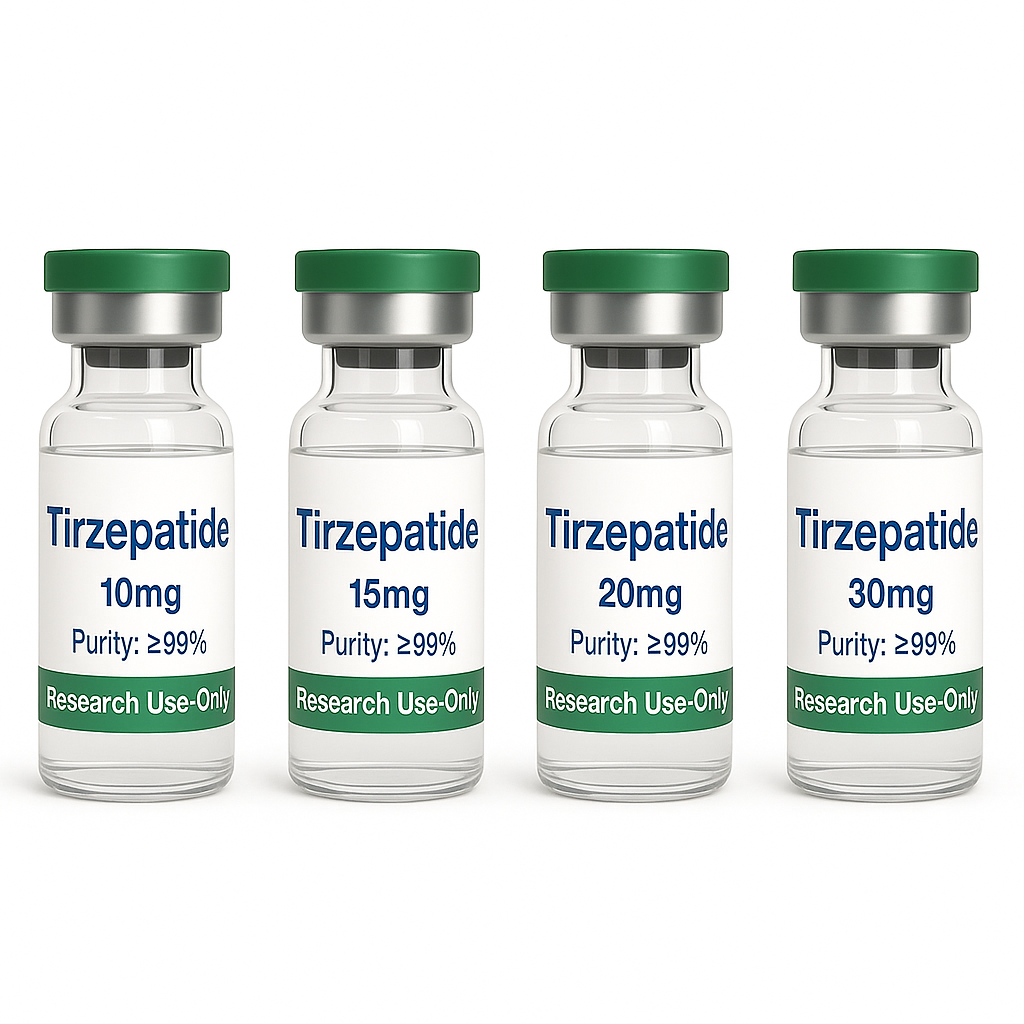
Tirzépatide lyophilisé, poudre de peptide de haute pureté (99 %), TR 10 mg, 15 mg, 20 mg, 30 mg par flacon pour le contrôle de la glycémie/diabète
Détails du produit
| Nom | Poudre injectable de tirzépatide |
| Pureté | 99% |
| Apparence | Poudre lyophilisée blanche |
| Administration | Injection sous-cutanée |
| Taille | 10 mg, 15 mg, 20 mg, 30 mg |
| Eau | 3,0% |
| Avantages | Traiter le diabète, améliorer le contrôle de la glycémie |
Description
Le tirzépatide est un nouvel agoniste des récepteurs du polypeptide insulinotrope glucose-dépendant/peptide-1 de type glucagon (GLP-1), approuvé aux États-Unis en complément d'un régime alimentaire et d'une activité physique pour améliorer le contrôle glycémique chez les adultes atteints de diabète de type 2. Son utilisation est actuellement étudiée dans la prise en charge du poids à long terme, la prévention des événements cardiovasculaires indésirables majeurs et le traitement d'autres affections, notamment l'insuffisance cardiaque à fraction d'éjection préservée, l'obésité et la stéatohépatite non alcoolique non cirrhotique. Le programme d'essais cliniques de phase 3 SURPASS 1-5 a été conçu pour évaluer l'efficacité et la sécurité du tirzépatide (5, 10 et 15 mg) administré par voie sous-cutanée une fois par semaine, en monothérapie ou en association, chez un large éventail de patients atteints de diabète de type 2. L'utilisation du tirzépatide dans les études cliniques a été associée à des réductions marquées de l'hémoglobine glyquée (de -1,87 % à -2,59 %, soit de -20 à -28 mmol/mol) et du poids corporel (de -6,2 à -12,9 kg), ainsi qu'à des réductions de paramètres généralement associés à un risque cardiométabolique accru, tels que la pression artérielle, l'adiposité viscérale et les triglycérides circulants. Le tirzépatide a été bien toléré, avec un faible risque d'hypoglycémie lorsqu'il est utilisé seul ou sans insulino-sécrétagogue, et a présenté un profil de sécurité globalement similaire à celui des agonistes des récepteurs du GLP-1. Par conséquent, les données issues de ces essais cliniques suggèrent que le tirzépatide offre une nouvelle option thérapeutique pour la réduction efficace de l'hémoglobine glyquée et du poids corporel chez les adultes atteints de diabète de type 2.