Le 24 août 2021, Cara Therapeutics et son partenaire Vifor Pharma ont annoncé que leur agoniste des récepteurs opioïdes kappa, le difelikefalin (KORSUVA™), premier de sa classe, avait reçu l'approbation de la FDA pour le traitement des patients atteints d'insuffisance rénale chronique (IRC) présentant un prurit modéré à sévère sous hémodialyse. Son lancement est prévu pour le premier trimestre 2022. Cara et Vifor ont signé un accord de licence exclusif pour la commercialisation de KORSUVA™ aux États-Unis et ont convenu de le vendre à Fresenius Medical. Cara et Vifor se partagent respectivement 60 % et 40 % des bénéfices des ventes réalisées hors Fresenius Medical, et 50 % des bénéfices réalisés avec ce dernier.
Le prurit associé à l'insuffisance rénale chronique (IRC-aP) est un prurit généralisé, fréquent et intense, chez les patients atteints d'IRC sous dialyse. Il touche environ 60 à 70 % des patients dialysés, dont 30 à 40 % présentent un prurit modéré à sévère, altérant considérablement leur qualité de vie (par exemple, en perturbant le sommeil) et pouvant être associé à la dépression. Jusqu'à présent, il n'existait aucun traitement efficace contre le prurit lié à l'IRC. L'autorisation de mise sur le marché de la difélikefaline contribue à combler un besoin médical important. Cette autorisation repose sur deux essais cliniques pivots de phase III inclus dans la demande d'autorisation de mise sur le marché : des données positives issues des essais KALM-1 et KALM-2 menés aux États-Unis et dans le monde, ainsi que des données complémentaires provenant de 32 études cliniques supplémentaires, démontrant la bonne tolérance de KORSUVA™.
Il y a peu, une bonne nouvelle est parvenue des chercheurs japonais concernant l'étude clinique sur la difélikefaline : le 10 janvier 2022, Cara a annoncé que ses partenaires, Maruishi Pharma et Kissey Pharma, ont confirmé l'utilisation de la difélikefaline injectable au Japon pour le traitement du prurit chez les patients hémodialysés. Lors des essais cliniques de phase III, le critère d'évaluation principal a été atteint. 178 patients ont reçu de la difélikefaline ou un placebo pendant 6 semaines et ont participé à une étude d'extension en ouvert de 52 semaines. Le critère d'évaluation principal (variation du score sur l'échelle numérique d'évaluation du prurit) et le critère d'évaluation secondaire (variation du score de démangeaisons sur l'échelle de sévérité de Shiratori) ont montré une amélioration significative par rapport à l'inclusion dans le groupe difélikefaline comparativement au groupe placebo, et le traitement a été bien toléré.
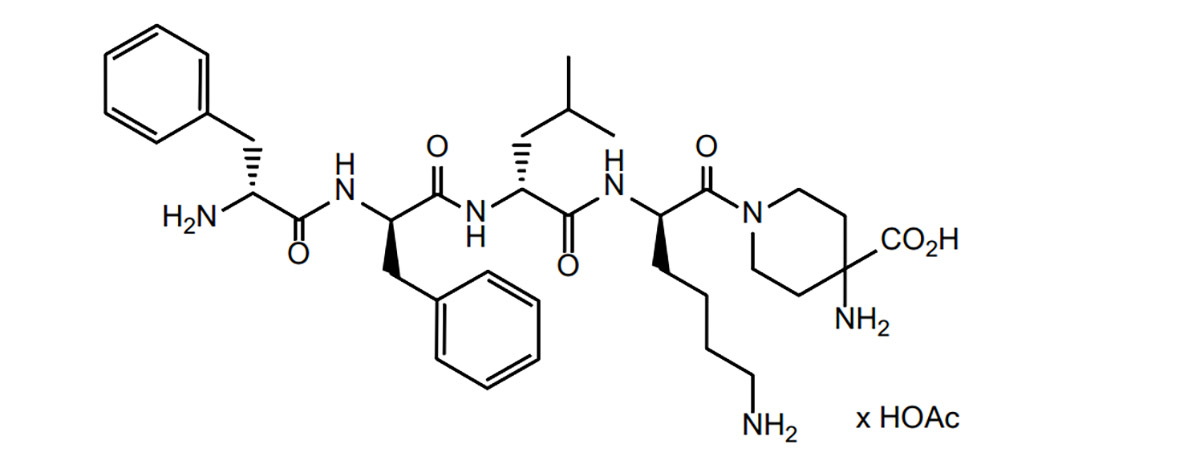
La difelikefaline appartient à une classe de peptides opioïdes. À partir de là, l'Institut de recherche sur les peptides a étudié la littérature scientifique sur les peptides opioïdes et a synthétisé les difficultés et les stratégies liées à leur utilisation dans le développement de médicaments, ainsi que l'état actuel de ce développement.
Date de publication : 17 février 2022